Après avoir présenté en détail la vitamine D, je continue cette fois-ci avec la vitamine B12, tout autant méconnue, et souvent sujet de discussion en soirée quand il y a un végétalien dans le coin :
Et la B12, c’est important, toussa toussa
Tu vas mourir ou terminer carencé en B12
Si la B12 n’existait pas je serais vegan moi aussi !
Dans ce dossier, découverte de la vitamine B12 ; de quoi devenir expert et pouvoir alimenter les discussions en soirée, autour un verre de vin vegan.
Ceux ne souhaitant pas lire l’intégralité du dossier devraient quoi qu’il en soit consulter le septième chapitre, discutant des carences en vitamine B12.
Voici les points que je vais aborder dans ce dossier :
- Vitamine B12 : introduction
- Vitamine B12 : sources
- Modes de digestion, d’absorption, transport et stockage
- Modes d’action
- Métabolisme de la vitamine B12
- Recommendations
- Vitamine B12 : carences
- Toxicité
- Sources
![]()
Vitamine B12 : Introduction
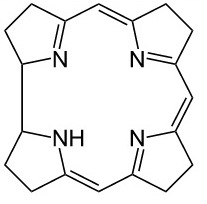
La vitamine B12, également appelée cobalamine n’est pas une vitamine à proprement parler, mais plutôt le regroupement d’un ensemble de corrinoïdes eux-mêmes qualifiés de macrocytes (qui sont des cycles formés par l’assemblage de 10 atomes ou plus). Ces corrinoïdes reposent sur un noyau corrine fait de quatre anneaux pyrroles liés :
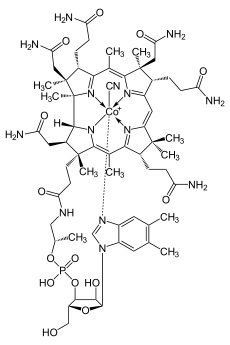
Le corrine de la vitamine B12 possède en plus un atome de cobalt en son centre auquel est attaché un nucléotide (qui est une molécule organique), le dimethylbenzimidazole. En plus de ce nucléotide, sont rattachés six autres groupes :
- -CN
- -OH
- -H2O
- -NO2
- 5′-Désoxyadénosine
- -CH3
C’est ce groupement que l’on nomme cyanocobalamine. Dans le schéma présenté, on peut voir le noyau corrine,ainsi que les groupements supplémentaires :
Vitamine B12 : sources
Les seules sources de vitamine B12 proviennent du royaume animal ; et les animaux eux-mêmes la dérivent en fait de micro-organismes. La totalité de la vitamine B12 disponible est produite par des micro-organismses. Il en est de même pour les végétaux ; si des sources de vitamine B12 sont décelées dans un végétal, alors elle est soit parvenue par contamination avec des micro-organismes ; ou bien encore grâce à des bacteries que l’on nomme « bactéries fixatrices d’azote », situés aux nodosités d’une plante. Les nodosités sont des petites boursouflures se formant à la racine de plantes sous l’action de bactéries.
Il est aussi possible qu’une contamination soit présente aux mains d’un individu ; et porter en bouche cette même nourriture peut permettre la transmission de vitamine B12.
Les meilleures sources de vitamine B12 sont les viandes, la volaille, certains crustacés, les oeufs (plus particulièrement le jaune d’oeuf). Dans les produits laitiers, la vitamine B12 présente diffère légèrement ; et est souvent présente en moins grande quantité ; elle est disponible sous la forme de méthyl– ainsi que d’ hydroxocobalamine. Enfin, il est également possible de trouver un peu de cyanocobalamine dans le tabac.
Commercialisée, elle est proposée sous deux formes :
- Cyanocobalamine
- Hydroxocobalamine
Cette forme est ensuite convertie dans le corps.
![]()
Modes de digestion, d’absorption, transport et stockage
Encore à ce jour, l’on ne sait pas véritablement comment la vitamine B12 est digérée et absorbée ; mais l’on sait que les cobalamines qui sont consommés sont dans un premier temps séparés des polypeptides auxquels ils sont rattachés ; et c’est dans l’estomac, sous l’action de l’acide chlorhydrique ainsi de la pepsine, enzyme protéolytique (enzyme capable de casser les protéines en plusieurs fragments) présents dans l’estomac, que le lien entre la vitamine et la nourriture à laquelle elle est rattaché est brisé.
C’est à partir de l’estomac, que deux protéines non-enzymatiques (la transcobalamine 1 ainsi que le facteur intrinsèque) jouent un rôle clé dans la digestion et l’absorption de la vitamine B12. La transcobalamine 2 (ou haptocorrines), présente dans la salive ainsi que le suc gastrique se fixe en amont sur la vitamine, alors présente sur les aliments protéiques.
Quant au facteur intrisèque, son action débute dans l’estomac pour se poursuivre dans le petit intestin.
Une fois la vitamine B12 détachée des aliments dans l’estomac, elle reste quoi qu’il en soit attachée aux transcobalamines, tout en se dirigeant vers la première partie du petit intestin. C’est au sein du duodénum que la transcobalamine est hydrolysée (décomposition par l’eau) par les protéases (ou peptidases), enzymes brisant les liaisons peptidiques des protéines, et c’est alors que de la cobalamine libre circule.
Il y a deux choses importantes à signaler à ce niveau :
- C’est une insuffisance en protéases qui limite la disponibilité en vitamine B12. Sans ces enzymes, le lien n’est pas brisée avec les transcobalamines, il n’est donc pas possible d’absorber la vitamine B12.
- Il semblerait que les transcobalamines jouent un rôle de protection de cette vitamine B12, en empêchant l’utilisation par les bactéries.
Dans l ‘intestin grêle proximal, le facteur intrinsèque, qui échappe à l’action des protéases, se lie à la cobalamine une fois que son lien avec la transcobalamine est rompu. Le facteur intrinsèque (IF en anglais) et la cobalamine se lient ensemble pour former un complexe : le cobalamine-facteur.
Ce complexe traverse alors la troisième et dernière partie du petit intestin, l’iléon pour atteindre des récepteurs sur lesquels la vitamine B12 se fixe :
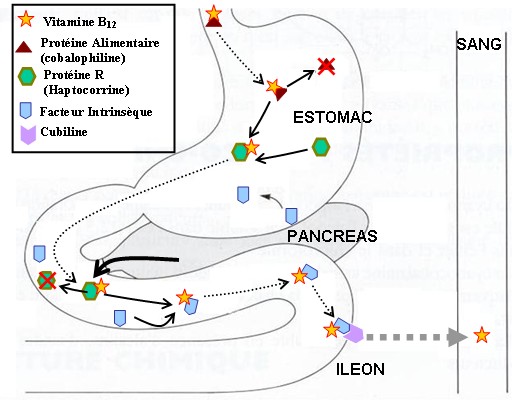 L’absorption et la digestion de la vitamine B12 sont encore des phénomènes peu compris, et il semblerait que l’absorption ne concerne que la vitamine transportée par le complexe ; et non le complexe cobalamine-facteur.
L’absorption et la digestion de la vitamine B12 sont encore des phénomènes peu compris, et il semblerait que l’absorption ne concerne que la vitamine transportée par le complexe ; et non le complexe cobalamine-facteur.
De plus, il semblerait que la mégaline, qui est une protéine, se fixe également au complexe, permettant ainsi le transport de la vitamine vers les cellules. Bien que la majorité de la vitamine B12 soit transportée au travers d’un récepteur spécifique, ce sont 1 à 3% de la vitamine B12 qui est absorbé par transport passif. Le transport passif désigne simplement le passage d’une molécule au travers d’une membrane sans apport d’énergie.
A ce jour ; on estime que la vitamine B12 est absorpée de l’ordre de 11 à 65 %, tout comme il a été montré que ce taux, chez un individu avec une bonne santé digestive, ne diminue pas.
De plus, une partie de cette vitamine B12 n’est pas directement transportée dans le sang, mais recyclé par le biais de la circulation entéro-hépatique. La CEH (je ne sais pas si l’acronyme existe ; soyons fous.) concernerait à peu près 1,4 µg par jour de cobalamine. Cela signifie que 1,4µg sont produits par la vésicule biliaire, et cette vitamine B12 peut à son tour se lier au facteur intrinsèque pour son absorption.
C’est donc une mauvaise absorption en premier lieu de la vitamine B12 qui augmente de facto les besoins en vitamine B12.
C’est au bout de 3 à 4 heures que la vitamine B12 apparait dans le sang, et les plus fortes concentrations sont présentes au bout de 4 à 8 heures. Dans le sang, on retrouve la vitamine B12 sous quatre formes :
- Méthylcobalamine : de 60 à 80% de la concentration.
- Adénosylcobalamine : 20% de la concentration.
- Cyanocobalamine
- Hydroxocobalamine
Dans la plasma sanguin la vitamine B12 en circulation, est liée à l’une des trois formes de transcobalamines : TC1, TC2 ou encore TC3. C’est un peu plus de 20% de la vitamine B12 dans le plasma qui est liée à la TC2, chargé de la transporter aux tissus concernés ; et à ce jour, le rôles des TC1 et TC3 sont encore inconnus à ce niveau. On pense que la TC3 permettrait le transport de la vitamine B12 des tissus au foi. Enfin 80% de la vitamine B12 est liée à la TC1, et il semblerait que ce complexe joue le rôle de stockage de vitamine B12 dans le plasma sanguin.
Le passage de la vitamine B12 dans les tissus ne se fait que par le biais de récepteurs spécifiques ; et tous les tissus sembleraient posséder des récepteurs pour la TC2. On pense que le complexe TC2-cobalamine pénètre les cellules pour ensuite fusionner avec les lysosomes (organites au sein des cellules) ; permettant la dégradation des TC2 et donc la libération de la vitamine au sein du cytosol :
C’est ensuite au sein de la cellule, que les différentes formes de vitamine B12 pourront êtres transformées, au besoin. Par exemple, par le biais d’une méthylation, l’hydroxocobalamine deviendra de la méthycobalamine.
Contrairement à la plupart des vitamines hydrosolubles ; la vitamine B12 peut être conservée dans le corps assez longtemps ; de l’ordre de quelques années. 2 à 4 mg sont stockés dans le foi ; mais la vitamine B12 peut également être présente en petites quantités dans les muscles, les reins, le coeur, le cerveau, la rate ou encore en circulation dans le sang. Dans le foi, elle est principalement stockée sous forme d’adénosylcobalamine ; et sous forme d’hydroxocobalamine ou méthylcobalamine ; mais en plus faibles quantités.
![]()
Modes d’action
A ce jour, il y a au moins deux réactions enzymatiques dépendantes de la vitamine B12. La première de ces réactions nécessite la vitamine B12 sous la forme de méthylcobalamine ; la deuxième sous forme d’ adénosylcobalamine. C’est la séquence d’un ensemble de réactions qui conduit à la production d’une liaiso carbone-cobalt entre le nucléus de la vitamine et l’un des ligands de méthyle ou de 5′-Désoxyadénosine.
La conversion de l’acide aminé homocystéine en methionine nécessite quand à elle la présence de méthylcobalamine en tant que co-enzyme. Cette réaction, en deux étapes, se produit dans le cytoplasme des cellules et consiste en :
- La liaison de cobalamine à la methionine synthase, qui se produit dans un premier temps ; et ce pour la formation de méthylcobalamine ; elle même nécessaire à la synthèse de methionine.
- Puis la méthylcobalamine, liée à l’enzyme methionine synthase , libère le groupe méthyle permettant le transfert vers l’homocystéine, produisant alors de la methionine et de la cobalamine.
La deuxième réaction enzymatique, qui requiert la vitamine B12 sous forme d’adénosylcobalamine, se produit dans les mitochondries cellulaires.
Avec une carence en vitamine B12, cette deuxième réaction enzymatique peut s’effectuer de manière incorrecte, conduisant à une augmentation d’acide méthylmalonique dans les fluides. C’est souvent la présence de cet acide méthylmalonique dans le sérum qui est mesuré pour déceller une carence en vitamine B12.
![]()
Métabolisme de la vitamine B12
La quasi-totalite de la vitamine B12 est dégradée avant son excrétion. Le renouvellement de la vitamine B12 est de l’ordre de 0,1% par jour, le gros de la vitamine excrété étant la vitamine liée aux transcobalamines au travers de la vésicule biliaire. Peu de vitamine B12 est excrétée via les urines ; et une petite partie se retrouve dans les peaux mortes.
![]()
Recommendations
Les recommendations en vitamine B12 se basent sur les estimations de vitamine B12 ingérée, et son renouvellement ; ainsi que sur la quantité nécessaire au maintien d’un niveau sérique normal.
A ce jour, on estime un besoin de 2,4 µg par jour, avec une augmentation allant de 0,2 à 0,4 µg par jour respectivement pour la femme enceinte et la femme allaitante.
Pour les adultes, on estime un besoin de 2,0 µg par jour. Pour les personnes âgées de 51 ans ou plus ; il est souvent recommendé la consommation d’aliments enrichis en vitamine B12, ou encore une supplémentation ; et ce parce que les changements du tractus gastro-intestinal, inhérents à l’âge, pourraient limiter la capacité d’absorption de la vitamine B12 (pour être plus précis, c’est l’affaiblissement de l’activité des enzymes permettant de récupérer la vitamine B12 rattachée aux aliments).
![]()
Vitamine B12 : carences
Une carence en vitamine B12 se manifeste par une anémie macrocytaire, qui est une diminution du taux d’hémoglobine dans le sang ; avec en plus la présence anormale dans le sang de cellules précurseurs des globules rouges, mais dont la taille est anormalement grande (ce qu’on appelle des mégaloblastes). La carence en vitamine B12 se manifeste en plusieurs étapes :
- Dans un premier temps, les concentration sériques diminuent, ce qui est observable par une diminution de la présence de transcobalamine 2.
- Dans un deuxième temps, la présence de vitamine B12 dans les cellules diminue.
- Dans un troisième temps, on parle de carence biochimique ; l’une des conséquence directe étant une diminution de la synthèse d’ADN ; ainsi qu’une augmentation dans le sang d’homocystéine et d’acide méthylmalonique.
- Enfin; les mégaloblastes (ces grosses globules rouges dont j’ai discuté plus haut) apparaissent, ainsi que l’anémie macrocytaire.
Parmi les signes visibles d’une carence en vitamine B12, citons :
- Troubles de la concentration
- Perte de mémoire
- Perte de l’orientation
- Sécrétions anormales des fibres myélinisées
- Fatigue
- Problèmes de peau
- Paralysies
- Palpitations
- Insomnies
- Fatigue
- Pâleur
Enfin, il faut savoir que pour 75 à 90% des individus concernés par une carence en vitamine B12, des problèmes neurologiques surviennent.
L’anémie macrocytaire peut être traitée avec l’admission de hautes doses de folates ; mais dans les cas de neuropathies, liés à la démyélinisation des nerfs (destruction de la gaine de myéline qui protège les nerfs) ; l’admission de folate s’avère hélas inefficace.
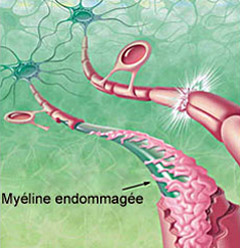
Les différents cas de neuropathie ne sont pas en fait liés qu’à une carence en vitamine B12, mais également aux enzymes liées , et une carence en vitamine B12 entraîne une diminution de l’activité des enzymes participant à son métabolisme et utilisation. Ces neuropathies pourraient êtres traitées avec un apport exogène de méthionine ou encore la production accrue de méthinonie depuis l’homocystéine , grâve à un apport supplémentaire en vitamine B12. C’est également une carence en vitamine B12 qui diminue la disponibilité en méthionine, et la diminution de méthionine entraîne une diminution de s-adénosylméthionine (SAM), métabolite chargé des réactions liées au transfert de méthyle ; et ces réactions sont nécessaires pour le maintien du fonctionnement de la myéline ; et donc le fonctionnement neurologique.
Il a été prouvé qu’une carence en SAM entraîne différentes neuropathies, comme par exemple dans le fluide cérébrospinal.
En plus de provoquer cette anémie, il semblerait que des niveaux élevés dans le plasma des concentrations d’homocystéine augmente le risque de maladies coronaires ; mais il est possible de diminuer ces mêmes concentrations avec l’admission de vitamine B6, de vitamine B12, ainsi que de folates.
Fait intéressant ; pour beaucoup de personnes souffrant de carences en vitamine B12 ; ça n’est pas tant la consommation de produits riches en vitamine B12 qui pose problème, sinon l’absorption de cette vitamine B12. L’exception étant les jeunes enfants, devenant végétaliens, pour lesquelles peu de vitamine B12 est stockée dans le corps.
A contrario, pour les adultes devenant végétaliens, le risque de souffrir de carence est bien moins important ; et ce parce que cette vitamine est stockée durant des années, en quantités suffisantes. Par précaution, il est cependant quoi qu’il en soit possible de se suppléer en vitamine B12.
Qu’est-ce qui peut être responsable de cette mauvaise absorption ?
- Et bien, dans un premier temps, certaines maladies auto-immunes, conduisant le corps à produire des anticorps attaquant les cellules gastriques produisant le facteur intrinsèque, requis pour le transport et l’absorption de la vitamine B12. Moins de FI signifie donc un transport et une absorption diminués.
- Citons également la gastrite atrophique, qui est une inflammation de la paroi interne de l’estomac, conduisant à une diminution également du FI. Les gastrectomies peuvent également êtres responsables d’une diminution de l’absorption de vitamine B12. Dans ces cas de gastrectomies, des anticorps sont produits ; et ces anticorps peuvent attaquer la pompe à protons. (la pompe à protons est un transporteur membranaire chargé du déplacement des protons au sein des cellules, permettant la diminution de son pH, entrainant donc une acidification).
- Une diminution d’acide chlorhydrique dans l’estomac peut également diminuer la rupture du lien entre une nourriture et la vitamine B21 rattachée.
- Les personnes ayant une paroi intestinale irritée ou la surface diminuée peuvent également souffrir d’une mauvaise absorption de la vitamine B12.
- Les personnes souffrant d’infection parasitaire intestinale peuvent également souffrir d’une mauvaise absorption, et ce parce que les parasites utilisent la vitamine B12.
- Mais aussi, la prise prolongée de bloqueurs H2 (antihistaminiques-H2) peut également conduire à une mauvaise absorption de la vitamine B12. Les bloqueurs H2 sont souvent prescripts pour les personnes souffrant d’ulcères à l’estomac ; leur rôle étant de réduire l’acidité dans l’estomac.
- D’autres inhibiteurs de la pompe à protons (IPP), ralentissant la production d’acide gastrique peuvent également diminuer l’absorption de la vitamine B12.
- Enfin ; signalons le protoxyde d’azote, utilisé en anesthésie peut dégrader la myéline chez l’individu déjà faiblement carencé en vitamine B12. Ce N2O inhibe l’acitivité de l’enzyme méthionine synthase en agissant avec le méthylcobalamine; ce qui peut potentiellement altérer la dégradation du cobalt.
Chez la personne âgée, on estime une carence de l’ordre de 15% et c’est l’admission de 6 à 9µg, et jusqu’à 300 µg de vitamine B12, qui sembleraient nécessaire pour pallier à ces carences.
Pour les cas plus sévères, comme l’anémie ou des carences liées à une mauvaise absorption, il est nécessaire de procéder à des injections répétées de vitamine B12 ; allant de 500 à 1000 µg ou encore l’ingestion orale de vitamine B12 allant jusqu’à 2mg par jour.
![]()
Toxicité
Bien qu’aucun cas de toxicité n’ait été rapporté ; signalons également qu’aucun bénéfice supplémentaire n’ait été découvert avec une sur-consommation de vitamine B12 chez l’individu bénéficiant d’un statut adéquat en vitamine B12 et vitamine B6.
![]()
Sources
- Anemia in inflammatory bowel disease: prevalence, differential diagnosis and association with clinical and laboratory variables.
- Vitamin B12 Deficiency in Inflammatory Bowel Disease: Prevalence, Risk Factors, Evaluation, and Management.
- [The risks of long-term proton pump inhibitors use].
- Urinary methylmalonic Acid as an indicator of early vitamin B12 deficiency and its role in polyneuropathy in type 2 diabetes.
- Proton pump inhibitor and histamine 2 receptor antagonist use and vitamin B12 deficiency.
- Vitamin B12:Dietary Supplement Fact Sheet
- The content, binding, and forms of vitamin B12 in milk
- Cobalamin, the stomach, and aging.
- Free and protein-bound cobalamin absorption in healthy middle-aged and older subjects.
- Structure-based perspectives on B12-dependent enzymes.
- Vitamin B12, folate, and homocysteine in depression: the Rotterdam Study.
- Spurious Elevations of Vitamin B12 with Pernicious Anemia